Tipificación del SDRA por COVID-19

Tipificación del SDRA por COVID-19
William Cristancho Gómez
A finales de 2019, se describió en China, un grupo de casos de neumonía de causa no identificada en ese momento, que después se reconocería como Síndrome Respiratorio Agudo Severo del Coronavirus 2 (SARS-CoV2),1-3 entidad conocida como enfermedad de coronavirus 2019 (COVID-19), la cual se asoció principalmente desde su primer reseña a trastornos respiratorios infecciosos de gravedad variable, dentro de los que, el Síndrome de Dificultad Respiratoria Agudo (SDRA) constituye el proceso mórbido más relevante y letal, cuyo manejo en el caso moderado/severo, es la ventilación mecánica invasiva.4-7
Para ser etiquetado el cuadro como SDRA, se utiliza actualmente la definición de Berlín (cuadro 1),8 en la que la relación PaO2/FiO2 es el principal marcador de gravedad, a diferencia de la anterior clasificación de Murray,9 en la que, la extensión por cuadrantes de los infiltrados alveolares en la radiografía de tórax, la distensibilidad, y el valor de la presión positiva al final de la espiración (PEEP) jugaban un rol importante en la tipificación del SDRA.
Cuadro 1. Definición de Berlín para el SDRA
|
Inicio |
Dentro de la primera semana de un insulto clínico conocido o síntomas respiratorios nuevos o que empeoran |
|
Imágenes del tórax |
Radiografía, tomografía computarizada o ultrasonido pulmonar: opacidades bilaterales no explicadas completamente por sobrecarga de volumen, colapso lobular o pulmonar o nódulos |
|
Origen de los infiltrados pulmonares |
Insuficiencia respiratoria no explicada completamente por insuficiencia cardiaca o sobrecarga de líquidos |
|
Deterioro de la oxigenación |
SDRA leve: PaO2/FiO2 ≤300 mm Hg (con PEEP o CPAP ≥ 5 cmH2O, o sin ventilación) SDRA moderado: PaO2/FiO2 ≤200 mm Hg (con PEEP ≥ 5 cmH2O, o sin ventilación) SDRA grave: PaO2/FiO2 ≤100 mm Hg (con PEEP ≥ 5 cmH2O, o sin ventilación) Cuando PaO2 no está disponible, SpO2/FiO2 ≤315 sugiere SDRA (incluso en pacientes no ventilados). |
PaO2: presión arterial de oxígeno, FiO2: fracción inspirada de oxígeno, SpO2: saturación periférica de oxígeno.
Es notable que, para clasificar el síndrome en uno de sus tres estadios, lo más relevante es el valor de la relación PaO2/FiO2. Sin embargo, no es el único parámetro de valoración, pues si así fuera, cualquier cuadro clínico que curse con hipoxemia –e incluso que aparezca tempranamente- podría ser SDRA. Entonces, cobran capital importancia las imágenes de tórax y el origen de las opacidades pulmonares, lo que quiere decir, que una imagen con presencia de infiltrados apoyaría el diagnóstico de SDRA tanto en la definición de Berlín, como en la clasificación de Murray; además la distensibilidad se encontrará disminuida, lo cual es característico y típico del SDRA. Quiere decir, que el síndrome cursa con una alteración de la llave distensibilidad/elasticidad, en la que existe fisiológicamente una relación inversa.10,11 Entonces la disminución de la primera significa necesaria e imperativamente un aumento de la segunda, y viceversa.
A finales de marzo de 2020, el grupo internacional de ventilación mecánica WeVent, publicó un “Protocolo respiratorio de paciente con SARS-COV-2 (COVID-19)”12 en el que se describe de una manera clara el manejo del paciente con SDRA por COVID-19 y se propone la tipificación del SDRA en dos cuadros diferentes: 1. El SDRA clásico que guarda correspondencia con la clasificación de Berlín, y 2. El SDRA con predominio de alteración del reflejo de vasoconstricción pulmonar hipóxica (VPH) que debe ser considerado en un paciente con pocos infiltrados alveolo-intersticiales (radiografía radiolúcida) y una pobre respuesta a las técnicas de reclutamiento. Este VPH es una contracción refleja del músculo liso vascular en la circulación pulmonar en respuesta a una baja presión parcial regional de oxígeno y constituye un mecanismo importante para el equilibrio de la relación entre la ventilación en el pulmón (V) y la perfusión regional en el área (Q), es decir en la relación V/Q.13 Desde el punto de vista de la fisiología respiratoria, el VPH por definición se estimula por hipoxia, un mecanismo fisiológico protector que desvía el flujo sanguíneo de las áreas hipóxicas de los pulmones a áreas con mejor ventilación y oxigenación; y se inhibe por el uso de una FiO2 innecesariamente alta lo que no solo puede contribuir a la atelectasia por absorción, sino que en áreas bien ventiladas al estar inhibido produce disminución de la relación V/Q por aumento de la perfusión agregada desde zonas hipóxicas y mal ventiladas (figura 1),13 lo cual agrava la hipoxemia, es decir, se anula el mecanismo de compensación.
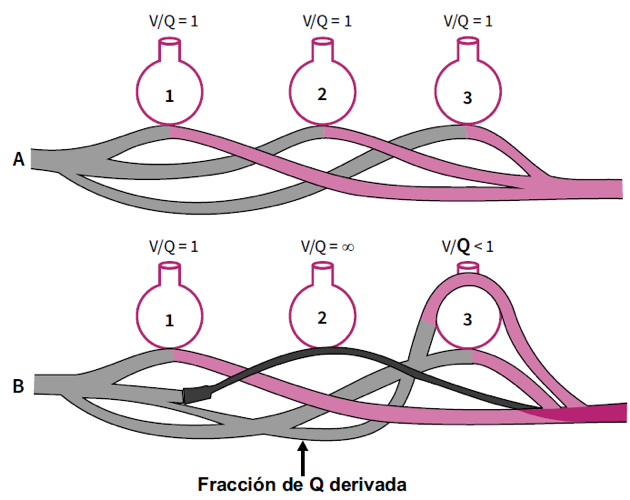
Figura 1. Representación de la ineficacia de la derivación de una fracción del Q hacia zonas funcionales en casos de elevación primaria de la relación V/Q. En A se representa la situación normal. En B se anula la perfusión hacia la unidad 2 por una enfermedad que cursa con incremento del espacio muerto (p. ej., tromboembolismo pulmonar), lo cual genera aumento ineficaz en la relación V/Q. El flujo sanguíneo (Q) se deriva hacia la unidad 3, en donde la perfusión excede a la ventilación produciendo disminución local de la V/Q con sus consecuencias (hipoxemia principalmente). Tomada de Cristancho W. Oxígeno. Fisiología, terapéutica, toxicidad. Colombia: Editorial El Manual Moderno, 2019.
En razón con lo expuesto, es irrefutable el concepto de SDRA clásico anotado, pero es conveniente replantear conceptualmente el de SDRA con predominio de alteración del reflejo de vasoconstricción pulmonar hipóxica (VPH), por tres razones incompatibles con el SDRA: 1. La distensibilidad es normal e incluso se sugiere que puede estar ligeramente aumentada; 2. Las imágenes diagnósticas exhiben alteraciones mínimas y; 3. El manejo propuesto incluye valores de PEEP iguales o menores a 10 cmH2O, cifra que no concuerda con el manejo convencional del SDRA. Podría tratarse de una Insuficiencia Respiratoria Aguda Tipo 1 (IRA 1), cuya causa es la pérdida del VPH que produce alteración marcada en la relación V/Q, como se describió antes, o se trate de una neumonía no severa, o tal vez, sea necesario revisar la clasificación de Berlín, o quizás se trate de un conflicto semántico.
Después de la publicación del WeVent, aparece el informe de Gattinoni et al.,14 en el que, se describen dos fenotipos de SDRA, uno denominado “L” (low) y otro “H” (high), lo cual refuerza la propuesta del WeVent. El fenotipo L (guarda similitudes con el SDRA con alteración del VPH), se caracteriza por baja elastancia (es decir, alta distensibilidad), baja relación V/Q, bajo peso pulmonar y baja capacidad de reclutamiento y el Tipo H (similar al SDRA clásico), se caracteriza por alta elastancia (es decir baja distensibilidad), alta derivación de derecha a izquierda (shunt), alto peso pulmonar y alta capacidad de reclutamiento. A partir de esta caracterización queda claro que el tratamiento dependerá del fenotipo, pero también se infiere que, el tipo L no es en esencia SDRA pues cursa con compliance de normal a alta, exhibe una baja relación V/Q, al igual que muchas anomalías pulmonares, posee un bajo peso pulmonar y carece de buena capacidad de reclutamiento, esto último podría deberse a dos extremos contrapuestos: normalidad relativa en la aireación o condensación del parénquima pulmonar; la distensibilidad normal o alta apoyaría la primera opción.
Después, en un editorial de Critical Care, Gattinoni et al.,15 modifican su postura y replantean la tipificación reforzando la de WeVent, puesto que proponen la presencia de dos tipos de pacientes en el contexto del COVID-19: pacientes tipo 1 sin SDRA y pacientes tipo 2 con SDRA, los cuales se diferencian por tomografía computarizada o por medición de sustitutos como el cálculo de la distensibilidad y la respuesta a PEEP. Según los autores, los pacientes tipo 1 exhiben disociación entre la gravedad de la hipoxemia -probablemente debida a la pérdida de vasoconstricción pulmonar hipóxica y la regulación alterada del flujo sanguíneo pulmonar- y el mantenimiento de una mecánica respiratoria relativamente buena. Es en últimas, una alteración de la relación V/Q cuyo manejo incluye la ventilación en prono, no para reclutar, sino para redistribuir la perfusión pulmonar, mejorando la relación V/Q. Los pacientes tipo 2 presentan baja distensibildiad, hipoxemia grave, menor aireación alveolar y mayor capacidad de reclutamiento, es decir, por definición, SDRA.
Un escenario que confiere gravedad a la neumonía por COVID-19 y al SDRA se relaciona con la aparición de fenómenos embólicos; se ha encontrado que, la embolia pulmonar aguda es una causa de deterioro clínico en las neumonías virales.16 El COVID-19 puede predisponer a la enfermedad tromboembólica venosa y arterial debido a inflamación excesiva, hipoxia, inmovilización y coagulación intravascular diseminada (CID).17-20 Es lógico deducir que, si se presenta un evento tromboembólico en el pulmón de un paciente con SDRA causado por COVID-19, la condición crítica se agravará, puesto que, al síndrome caracterizado por aumento del corto circuito pulmonar se agregará una grave enfermedad de espacio muerto, y si el cuadro es leve evolucionará tórpidamente, lo que podría ocurrir en pacientes con etiquetas diagnósticas similares al SDRA, tales como SDRA con predominio de alteración del reflejo de vasoconstricción pulmonar hipóxica (VPH), o SDRA tipo L, o pacientes Tipo 1 sin SDRA. Una revisión Cochrane de 4 estudios publicados hasta la fecha,21-24 encontró que en las series principales de pacientes con COVID-19 quienes tenían peor pronóstico exhibían niveles de dímero D mucho más altos que los pacientes con enfermedad menos grave y que un valor superior a 1.0 mg/L es uno de los principales factores de mal pronóstico. También se ha observado un mayor tiempo de protrombina entre los pacientes más graves.
Conclusiones
El cuadro clínico respiratorio asociado al COVID-19, puede presentarse como SDRA clásico, el cual puede tener tres estadios de gravedad (leve, moderado o severo) conforme a la definición de Berlín, o puede manifestarse como un cuadro de insuficiencia respiratoria aguda tipo 1 (IRA 1), es decir, IRA hipoxémica, la que ha sido llamada en las referencias citadas como, SDRA con predominio de alteración del reflejo de vasoconstricción pulmonar hipóxica (VPH), o SDRA tipo L, o pacientes Tipo 1 sin SDRA, las que se originan en desequilibrio de la relación V/Q por aumento del shunt, o por aumento del espacio muerto pulmonar como ocurre en los fenómenos embólicos. Es conveniente conservar los criterios aceptados universalmente para no generar confusión en la comunidad científica, hasta que se publique una nueva clasificación producto de un amplio consenso mundial.
REFERENCIAS
1. Zhu N, Zhang D, Wang W et al.: A novel coronavirus from patients with pneumonia in China, 2019. N Engl J Med 2020;382:727-733.
2. World Health Organization: Pneumonia of unknown cause — China. January 5, 2020 (https://www.who.int/csr/don/05-january-2020-pneumonia-of-unkown-cause-china/en/).
3. World Health Organization: Novel Coronavirus — China. January 12, 2020 (https://www.who.int/csr/don/12-january -2020-novel-coronavirus-china/en/). Consultado: marzo 27 de 2020.
4. Wujtewicz M, Dylczyk-Sommer A, Aszkiełowicz A et al.: COVID-19 - what should anaethesiologists and intensivists know about it? Anaesthesiol Intensive Ther 2020. pii: 40133. DOI: 10.5114/ait.2020.93756.
5. Australian and New Zealand Intensive Care Society: ANZICS COVID-19 Guidelines, 202, ANZICS: Melbourne.
6. Alhazzani W, Møller MH, Arabi YM, Loeb M, Gong MN, Fan E, Rhodes A et al.: Surviving Sepsis Campaign: guidelines on the management of critically ill adults with Coronavirus Disease 2019 (COVID-19). Intensive Care Medicine, 2020. DOI:10.1007/s00134-020-06022-5.
7. Du RH, Liang LR, Yang C-Q et al.: Predictors of Mortality for Patients with COVID-19 Pneumonia Caused by SARS-CoV-2: A Prospective Cohort Study. Eur Respir J 2020; in press (https://doi.org/10.1183/13993003.00524-2020). Consultado: abril 10 de 2020
8. Force ADT, Ranieri VM, Rubenfeld GD, Thompson BT, Ferguson ND, Caldwell E et al.: Acute respiratory distress syndrome: the Berlin Definition. JAMA. 2012;307(23):2526-33. Epub 2012/07/17. DOI: 10.1001/jama.2012.5669. PubMed PMID: 22797452.
9. Murray JF, Matthay MA, Luce LM et al.: An expanded definition of the adult respiratory distress syndrome. Am Rev Resp Dis 1988;139:720-723
10. West J, Luks A: Fisiología respiratoria: Fundamentos, 10ª edición. Barcelona: Wolters Kluwer, cop, 2016.
11. Cristancho W: Fisiología respiratoria. Lo esencial en la práctica clínica, 3ª edición. Colombia: Editorial El Manual Moderno, 2015.
12. WeVent: Protocolo respiratorio de paciente con SARS-COV-2 (COVID-19). Disponible en: https://www.formacionsanitaria.eu/index.php/es/wevent?fbclid=IwAR3-v_7JY2K9lRlnVOEIMy1uC5Lb28fML72Dsnrlt_eFHCRDHt1s5jZEmNY. Consultado: 20 marzo 2020.
13. Tarry D, Powell M: Hypoxic pulmonary vasoconstriction. BJA Education, 2017;17(6), 208–213. DOI:10.1093/bjaed/mkw076.
14. Gattinoni L et al.: COVID-19 pneumonia: different respiratory treatment for different phenotypes? Intensive Care Medicine, 2020. DOI: 10.1007/s00134-020-06033-2.
15. Gattinoni L, Chiumello D, Rossi S: COVID-19 pneumonia: ARDS or not? Critical Care 2020;24(4):154. DOI: https://doi.org/10.1186/s13054-020-02880-z.
16. Xie Y, Wang X, Yang P, Zhang S: COVID-19 Complicated by Acute Pulmonary Embolism. Radiology: Cardiothoracic Imaging 2020;2(2):e200067. DOI: https://doi.org/10.1148/ryct.2020200067.
17. Chen T, Wu D, Chen H et al.: Clinical characteristics of 113 deceased patients with coronavirus disease 2019: retrospective study, Bmj 2020;368:m1091.
18. Guan WJ, Ni ZY, Hu Y et al.: Clinical characteristics of coronavirus disease 2019 in China, N Engl J Med, 2020. DOI: https://doi.org/10.1056/NEJMoa2002032.
19. Wang D, Hu B, Hu C et al.: Clinical Characteristics of 138 Hospitalized Patients with 2019 Novel Coronavirus-Infected Pneumonia in Wuhan, China, Jama, 2020.
20. Zhou F, Yu T, Du R et al.: Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study, Lancet 2020;395:1054–1062.
21. Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, Zhang L, Fan G, Xu J, Gu X, Cheng Z, Yu T, Xia J, Wei Y, Wu W, Xie X, Yin W, Li H, Liu M, Xiao Y, Gao H, Guo L, XieJ, Wang G, Jiang R, Gao Z, Jin Q, Wang J, Cao B: Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet, 2020;395(10223):497-506. DOI: 10.1016/S0140-6736(20)30183-5.
22. Tang N, Li D, Wang X, Sun Z: Abnormal coagulation parameters are associated with poor prognosis in patients with novel coronavirus pneumonia. J Thromb Haemost. 2020;18(4):844-847. DOI: 10.1111/jth.14768.
23. Wang D, Hu B, Hu C, Zhu F, Liu X, Zhang J, Wang B, Xiang H, Cheng Z, Xiong Y, Zhao Y, Li Y, Wang X, Peng Z: Clinical Characteristics of 138 Hospitalized Patients With 2019 Novel Coronavirus-Infected Pneumonia in Wuhan, China. JAMA. 2020 Feb 7. DOI: 10.1001/jama.2020.1585.
24. Zhou F, Yu T, Du R, Fan G, Liu Y, Liu Z, Xiang J, Wang Y, Song B, Gu X, Guan L, Wei Y, Li H, Wu X, Xu J, Tu S, Zhang Y, Chen H, Cao B: Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020;395(10229):1054-1062. DOI: 10.1016/S0140-6736(20)30566-3.

